MCrAlY(M 为 Ni、Co 或 NiCo)涂层是20世纪80年代发展起来的第三代高温防护涂层,不仅具有良好的抗高温氧化和热腐蚀性能,同时兼具良好的抗热疲劳性能和韧性,是一种较为理想的高温防护涂层。MCrAlY涂层的制备方法主要有磁控溅射(Magnetron sputtering,MS)[1]、电弧离子镀(Arc ion plating,AIP)[2–3]、电子束物理气相沉积(Electron beam physical vapor deposition,EB–PVD)[4]、超音速火焰喷涂(High velocity oxy-fuel spraying,HVOF)[5]、低压等离子喷涂(Low pressure plasma spraying,LPPS)[6–7]等。MCrAlY 涂 层 具 有良好的综合性能,既可以单独作为高温防护涂层使用,也可以作为热障涂层体系中的粘结层来使用。然而,在更高温度下(≥1100 ℃),由于涂层中Al含量不足,传统MCrAlY涂层抗氧化性能较差,为提高其服役寿命,研究人员对MCrAlY的成分和结构进行改性。Lu等[8]在NiCoCrAlY涂层表面进行渗铝处理,得到了外层富Al的梯度涂层,由于Al含量的大幅提升,该涂层表现出更好的抗高温氧化性能。此外,研究人员还在涂层中引入了Pt、Ta等元素进行成分改性,使得涂层的抗氧化性能及氧化膜的抗剥落性能均得到有效提高[9–10]。典型的结构改性是通过工艺来优化涂层的组织结构,如MS制备的涂层,其结构为柱状纳米晶,其内部存在大量的晶界能够显著降低Al选择性氧化所需的临界浓度;AIP在较低偏压制备的涂层具有柱状结构,高偏压下涂层则会呈现层状生长[11–12]。理想的高温防护涂层应满足: (1)与基体之间的互扩散较小; (2)维持热生长氧化物(Thermally grown oxide,TGO)具有较低的生长速率; (3)生成的TGO应具有良好的抗剥落性能和耐磨性[13]。金属陶瓷综合了金属与陶瓷的优点,既具有金属良好的热稳定性和韧性,同时又具备陶瓷材料的耐高温及耐磨损的特性,展现出巨大的应用潜力。电镀和喷涂技术是金属陶瓷涂层常用的制备工艺。Tan等[14]通过电镀在铝化物涂层中掺杂了CeO2颗粒,CeO2掺杂对铝化物涂层的氧化动力学具有两方面的协同作用: (1)CeO2颗粒抑制了θ–Al2O3向α–Al2O3的转变; (2)溶解在氧化膜中的Ce4+偏聚在氧化膜晶界处,抑制了Al3+的扩散,从而降低了氧化膜的生长速率。Bolelli等[15]使用等离子喷涂技术在NiCrAlY涂层中掺入Al2O3颗粒,有效提高了NiCrAlY涂层常温下的耐磨性。相较于电镀和喷涂技术,MS和AIP技术制备金属陶瓷涂层具有显著的优势。这是因为MS和AIP在涂层制备过程中可通过对反应气体的压强和流量的调整有效控制涂层中陶瓷相的含量。此外,MS和AIP制备的涂层陶瓷颗粒分布更加均匀、弥散。Zhu等[16–21]通过物理气相沉积的方法,在涂层沉积的过程中通入反应气体N2或O2制备的金属陶瓷涂层,具有热膨胀系数小、晶粒尺寸小等特点,且抗氧化性能和力学性能上均得到了一定提升。如通过AIP在NiCrAlYSi涂层中引入了氮化物颗粒,可有效降低涂层的热膨胀系数,且具有更好的抗循环氧化性能[13]。虽然研究人员对NiCrAlY基纳米金属陶瓷涂层进行了大量研究,但纳米金属陶瓷涂层的高温氧化测试温度始终局限于传统MCrAlY涂层的服役温度(≤ 1050 ℃ [22–23]),关于纳米金属陶瓷涂层在更高温度下的氧化特点却鲜有报道。本文将对不同O掺杂含量的纳米金属陶瓷涂层在更高温度下(1100 ℃)的氧化性能进行研究。
1 试验及方法
1.1 样品制备
试验采用二代单晶N5作为基体材料,使用多弧离子镀(DH–4,辽宁北宇真空科技有限公司)制备NiCrAlYN和NiCrAlYN+O纳米金属陶瓷涂层。基体N5和涂层制备所使用靶材的名义成分如表1所示。在制备涂层前,使用线切割将单晶试棒切成尺寸为φ15 mm×2 mm的试片,使用SiC砂纸打磨至2000#后,再用丙酮和酒精混合溶液超声清洗10 min,吹干待用。将试片悬挂在样品架上并以10 r/min的速度自转,靶材与样品间距为200 mm。制备涂层前,先将真空室内背底真空度抽至 6.0×10–3 Pa以下。随后通入高纯Ar气至真空度为2.0~3.0 Pa,在偏压为–900 V,20%占空比的情况下进行Ar+溅射清洗3 min,去除样品表面的污染。样品清洗完成后,关闭Ar气,通入高纯N2和O2作为反应气体制备纳米金属陶瓷涂层。详细试验参数如表2所示,将O2通入量为0的涂层命名为C(N),通入量为10 sccm的涂层命名为C(N+10O),通入量为20 sccm的涂层命名为C(N+20O)。制备完成后的样品在真空退火炉中进行真空退火,退火处理能够促进涂层中的元素扩散,使涂层的组织、成分均匀化,愈合制备过程中涂层产生的孔洞、裂纹等缺陷。退火时当真空度低于6.0×10–3 Pa时开始加热,升温速率为7 ℃/min,在1000 ℃下保温6 h后随炉冷却至室温。恒温氧化测试在1100 ℃的马弗炉中进行,氧化时间为300 h。
表1 第二代镍基单晶高温合金N5和靶材NiCrAlY的名义成分(质量分数)
Table 1 Nominal compositions of N5 single crystal superalloy and NiCrAlY target(mass fraction) %
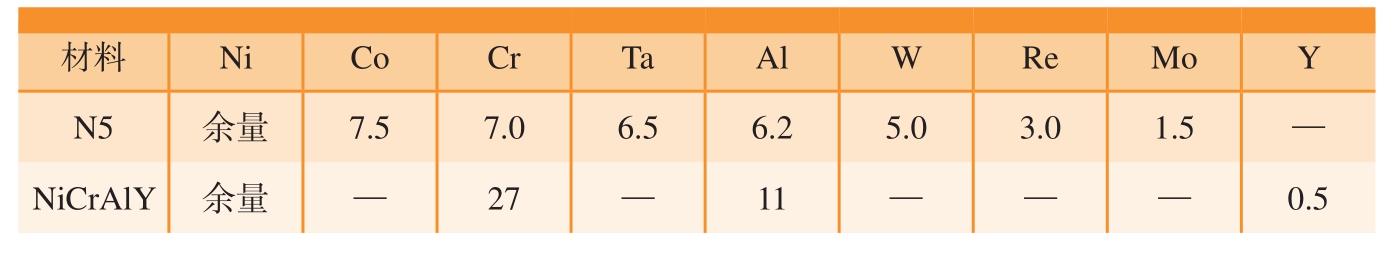
材料 Ni Co Cr Ta Al W Re Mo Y N5 余量 7.5 7.0 6.5 6.2 5.0 3.0 1.5 —NiCrAlY余量— 27— 11— — — 0.5
表2 纳米金属陶瓷涂层的制备参数
Table 2 Preparation parameters of nano-cermet coatings
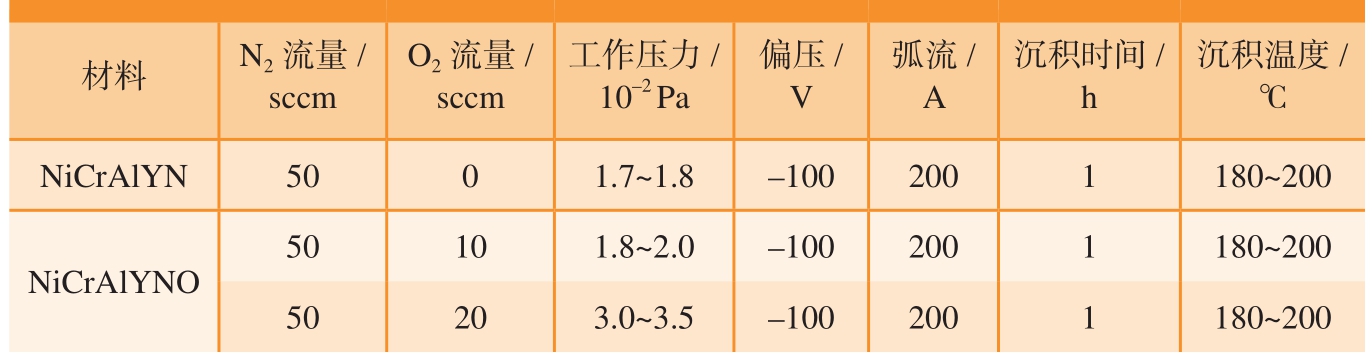
沉积温度/℃NiCrAlYN 50 0 1.7~1.8 –100 200 1 180~200材料 N2流量/sccm O2流量/sccm工作压力/10–2 Pa偏压/V弧流/A沉积时间/h NiCrAlYNO 50 10 1.8~2.0 –100 200 1 180~200 50 20 3.0~3.5 –100 200 1 180~200
1.2 表征方法
采用X射线衍射仪(X’ Pert PRO,PANalytical Co.,加速电压为40 kV时, Cu–Kα辐射)对涂层的制备态、退火态和氧化态进行物相分析。使用扫描电子显微镜(InspectF 50,FEI Co.)和能谱仪(INCA X–MAX,Oxford Instruments Co.)对样品的表面、截面形貌和成分进行分析。
2 结果与讨论
2.1 涂层的制备态、退火态组织结构
图1(a)~(c)分别是3种涂层沉积态的表面形貌,可知3种涂层表面均呈现出典型的菜花状形貌,存在明显的大溶滴。图1(d)~(f)分别是3种涂层沉积态的截面图,涂层的平均厚度约为22 μm,可以看出,涂层中存在大量纵向和横向裂纹,这主要是由于AIP在沉积过程中靶面蒸发出大量的大溶滴沉积在样品表面所造成的,这种缺陷经真空退火可以完全消除,涂层与基体之间结合紧密,未见明显的局部分离区(Local detachment regions,LDR)。图2为3种沉积态涂层的XRD衍射图谱,衍射峰明显宽化,表明涂层晶粒尺寸的细化。可以看出,涂层主要的相组成为γ/γ'相,没有检测到明显的氮化物或氧化物的衍射峰。本研究前期工作表明N、O元素的掺杂会在涂层中形成3种亚稳的氮化物fcc–AlN、fcc–CrN和Cr2N以及一种刚玉结构的氧化物(Al,Cr)2O3,可能伴随少量的Y2O3和NiO[24]。由于N、O元素掺杂量少,生成的陶瓷颗粒含量较少,因此XRD难以检测。

图1 3种沉积态涂层的表面形貌及截面形貌
Fig.1 Surface morphology and cross-sectional morphology of three as-deposited coatings
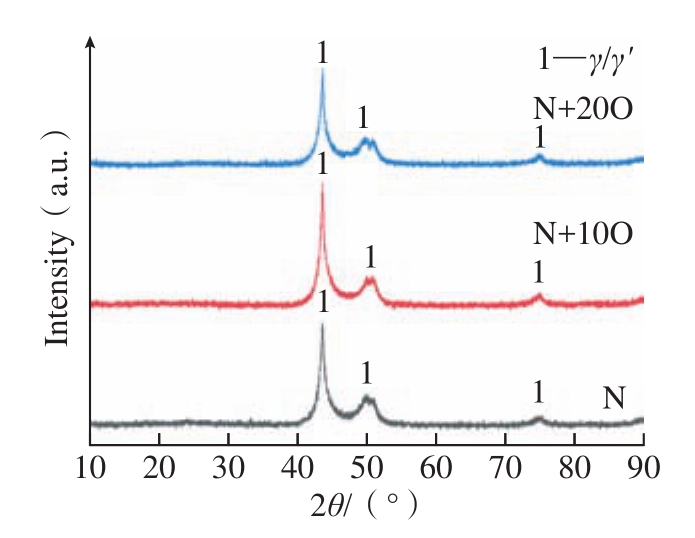
图2 3种沉积态涂层的XRD图谱
Fig.2 XRD patterns of three as-deposited coatings
图3为1000 ℃真空退火6 h的样品表面及截面形貌图。从图3(a)~(c)3种样品的表面形貌可以看出,表面依旧存在大量的溶滴颗粒,与退火前的样品表面形貌相似。但是从图3(d)~(f)3种样品退火截面图可以看出,原本沉积态涂层中存在的大量裂纹孔洞在退火之后明显愈合,涂层内部变得完整致密。退火后涂层内部析出大量细小弥散的陶瓷颗粒,且随着沉积过程中O含量的增多,涂层中出现了陶瓷颗粒聚集的现象,如C(N+20O)涂层中出现了大颗粒陶瓷相的析出,如图3(f)中箭头所指,其成分为Ni–40.48Cr–18.75Al–5.39N(质量分数,%)。图4为3种涂层退火态的XRD衍射图谱,衍射峰明显变窄,说明退火过程中晶粒迅速长大。分析发现,原本沉积态涂层的 γ/γ'主相转变为 γ/γ'、α–Cr相以及极少含量的β–NiAl相(衍射峰十分微弱,未在图4中标出),同时在3种涂层的衍射图谱中均检测到微弱的AlN衍射峰。经计算沉积态涂层中可能含有物相在1000℃下标准摩尔吉布斯自由能:AlN为 –179.649 kJ/mol,CrN 为 –20.694 kJ/mol,Cr2N 为 –31.315 kJ/mol,NiO为–124.976 kJ/mol,Cr2O3为–803.042 kJ/mol,Al2O3为 –1270.513 kJ/mol。因此在1000 ℃退火过程中可能会发生以下反应。

图3 3种退火态涂层的表面形貌及截面形貌
Fig.3 Surface and cross-sectional morphology of three annealed coatings
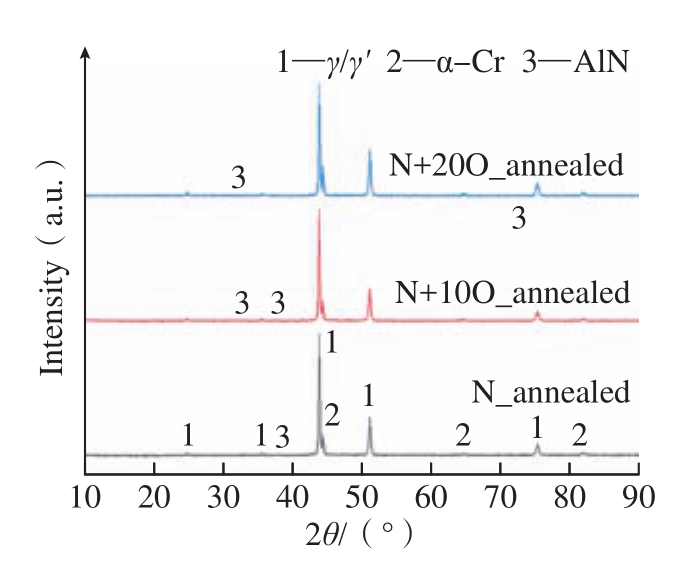
图4 3种退火态涂层的XRD图谱
Fig.4 XRD patterns of three annealed coatings
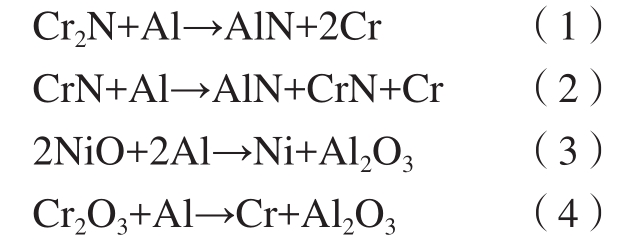
所以,在退火过程中CrN和Cr2N颗粒会转变为AlN颗粒,析出α–Cr相,使AlN含量增加,因此在图4退火态XRD图谱中能够检测到α–Cr峰和微量的AlN峰。同时亚稳的NiO和Cr2O3颗粒将转变为Al2O3颗粒。
2.2 高温氧化测试
图5(a)~(c)是 3种样品在1100 ℃下恒温氧化300 h的表面形貌。可以看出样品表面氧化膜均发生了一定程度的剥落,相较于C(N)和C(N+10O)涂层,C(N+20O)涂层表面氧化膜剥落较轻微。C(N+20O)剥落坑形貌与未剥落区相似。C(N)和C(N+10O)涂层表面剥落区则呈现明显的疏松结构。对三者的剥落坑进行元素分析,具体成分如表3所示。可以看出,随着掺杂O元素的增多,剥落区域的Ni、Cr元素的含量在逐渐减少,同时在剥落坑区域检测到了基体元素Co。结合图6的3种涂层氧化后的掠入射X射线衍射(Grazing incidence X–ray fraction,GI–XRD)图谱可以推测在 1100 ℃氧化300 h后样品表面均生成了NiAl2O4相。除尖晶石外,还在3种样品表面检测到 α–Al2O3和 γ/γ'的衍射峰,仅在C(N+20O)的样品表面检测到微弱的AlN信号。在样品表面并没有观察到AlN颗粒,推测AlN颗粒可能位于氧化膜的内部或下方。使用MDIJade 6软件对氧化产物的相对含量进行计算,表面生成的Al2O3与NiAl2O4的体积比C(N)为 69:31,C(N+10O)为 59.8:40.2,C(N+20O)为87.7:12.3。尖晶石相的生成会随着掺杂O含量的增加呈现先增加后减少的趋势。图5(d)~(f)是3种涂层在1100 ℃氧化300 h后的截面图,3种涂层的氧化膜平均厚度分别为 8.78 μm、7.9 μm 和 5.7 μm。可以看出C(N)和C(N+10O)涂层均存在较为严重的剥落,虽然C(N+20O)涂层样品表面同样存在一些剥落区域,但是截面上并不存在涂层和空气界面直接接触的情况。通过对氧化膜局部放大(图7(a)~(c))的观察发现,C(N)和C(N+10O)涂层的氧化膜发生了明显的分层,结合EDS和图6的XRD数据可判断上层浅灰色氧化物为NiAl2O4相。两者尖晶石层的厚度分别为1.77 μm和2.32 μm。而C(N+20O)并没有观察到明显的氧化膜分层,可能是尖晶石颗粒弥散分布在氧化膜中,这与MDIJade 6软件计算NiAl2O4相含量的结果符合。掺杂了O元素的涂层在真空退火过程中,涂层中的亚稳态氧化物颗粒Cr2O3和NiO等可与涂层中的金属Al发生式(3)和(4)的反应,在样品表面生成稳定的Al2O3颗粒。但由于C(N+10O)涂层中掺杂O含量较少,样品表面形成的Al2O3颗粒呈孤岛状分布,造成Al2O3孤岛附近局部贫Al,因此在氧化初期促进了尖晶石相的形成。相反C(N+20O)涂层氧化膜表面并没有生成明显的尖晶石相,可能是由于掺杂O含量较多,在真空退火后样品表面形成了较为完整的Al2O3薄膜,有效地隔绝了涂层与空气的接触,从而抑制了尖晶石相的生成。由于尖晶石结构的物质具有较大的生成氧化物分子体积与所消耗金属原子的体积比(Pilling-bedworth ratio,PBR)值,因此在生长过程中会产生较大的内应力,氧化膜将会通过变形、形成裂纹或是剥落来释放应力,因此C(N)和C(N+10O)出现了大量的氧化膜剥落,而C(N+20O)仅发生了轻微的剥落。
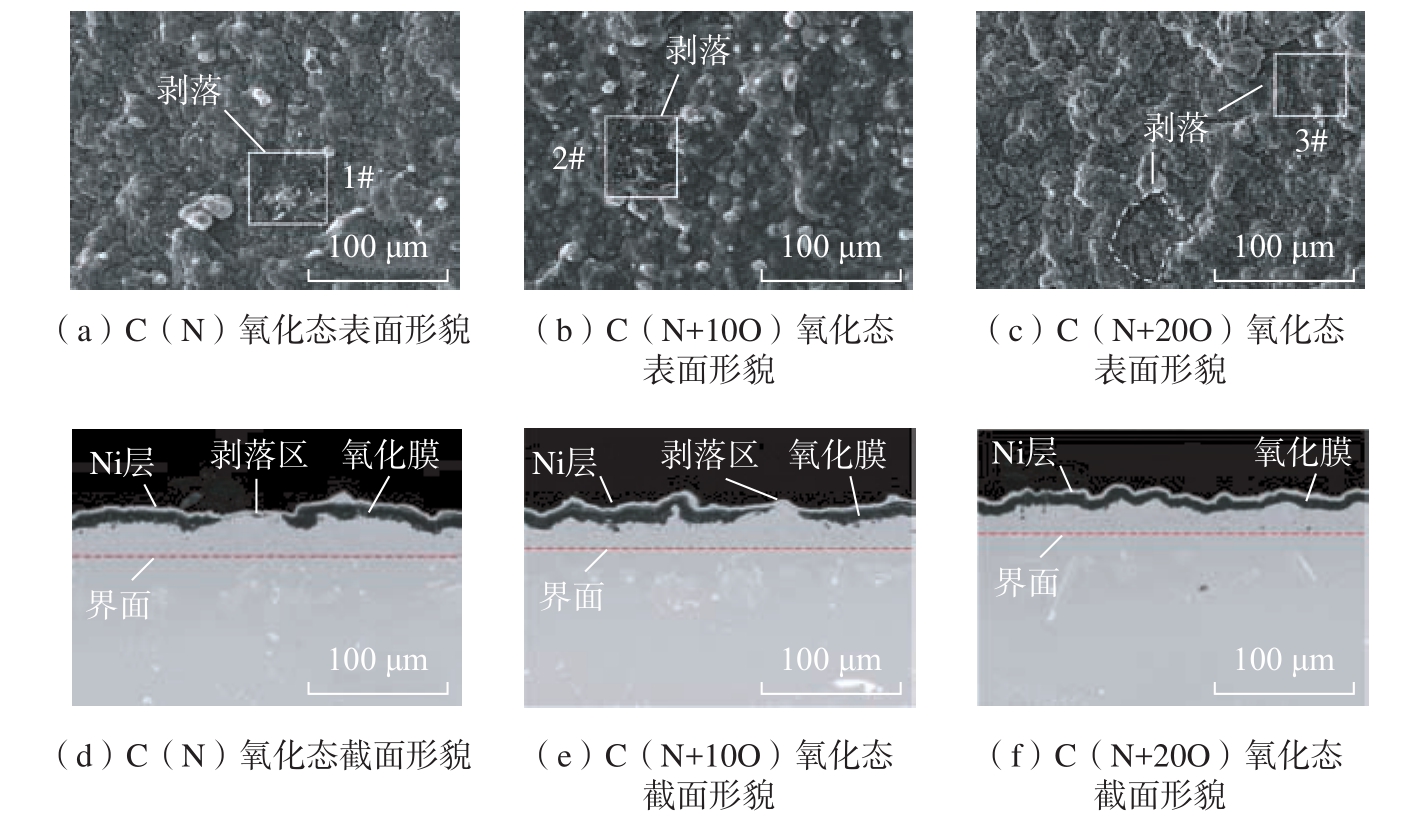
图5 经1100 ℃氧化300 h后3种涂层表面和截面形貌
Fig.5 Surface and cross-sectional morphology of three coatings after isothermal oxidation at 1100 ℃ for 300 h
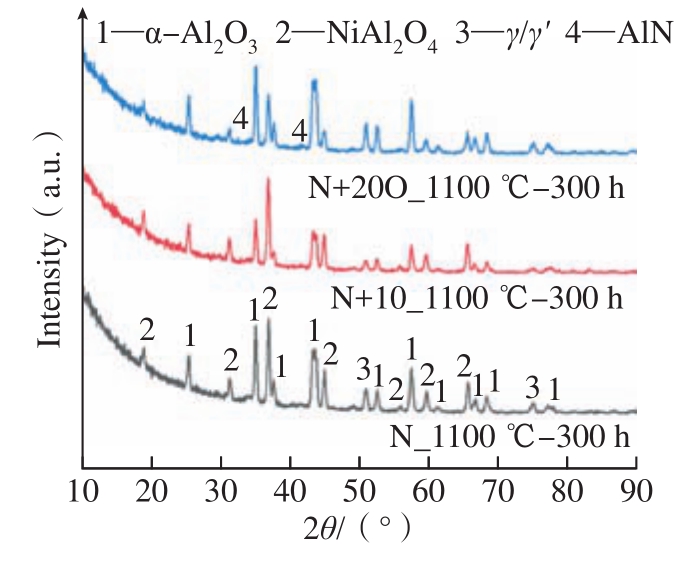
图6 3种涂层经1100 ℃氧化300 h后XRD图谱
Fig.6 XRD patterns of three coatings after isothermal oxidation at 1100 ℃ for 300 h
表3 氧化膜剥落区域化学成分(质量分数)
Table 3 Chemical composition of oxide film peeling area (mass fraction) %
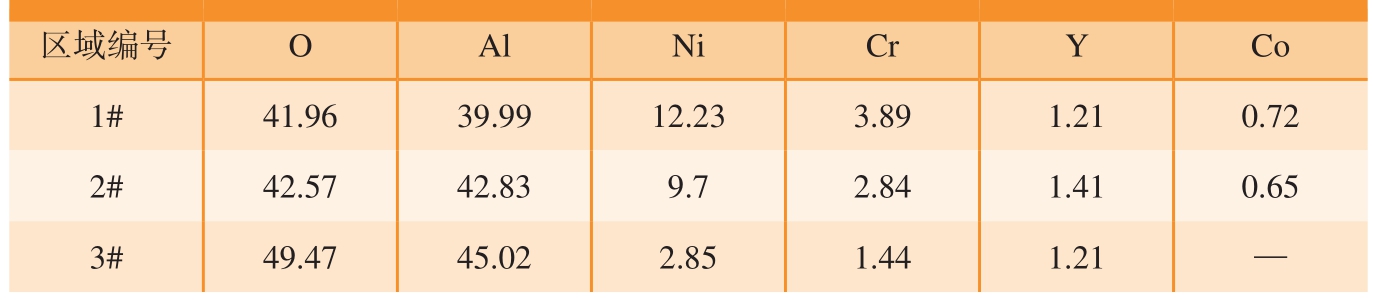
区域编号 O Al Ni Cr Y Co 1# 41.96 39.99 12.23 3.89 1.21 0.72 2# 42.57 42.83 9.7 2.84 1.41 0.65 3# 49.47 45.02 2.85 1.44 1.21 —
除此之外,三者的氧化膜中均含有大量的亮白色颗粒,经能谱分析可知氧化膜中的亮色颗粒为富Y颗粒,其主要成分如表4所示。图7(d)~(f)为涂层和氧化膜中的Y元素分布图,C (N) 涂层中富Y大颗粒较少,但氧化膜中存在明显的大颗粒夹杂。C(N+10O)和C(N+20O)涂层中随着掺杂O含量的提高能够显著减少涂层和氧化膜中富Y颗粒的团聚。Jia等[24]研究表明,涂层中的O元素对Y具有拖拽作用,当O含量较低时,Y会在涂层中形成团聚,并在氧化膜中形成大颗粒的Y3Al5O12氧化物夹杂,Y3Al5O12夹杂在氧化膜中会为O2–向内扩散提供快速扩散通道,因此会提高氧化膜的生长速率;但当O含量较高时,O对Y的拖拽作用增强,Y将以细小弥散的Y3Al5O12颗粒分布在涂层中,抑制大颗粒的Y–Al氧化物夹杂在氧化膜中形成,从而降低了氧化膜的生长速率。
表4 氧化膜中亮白色颗粒的化学成分(质量分数)
Table 4 Chemical composition of bright particles in oxide film (mass fraction) %
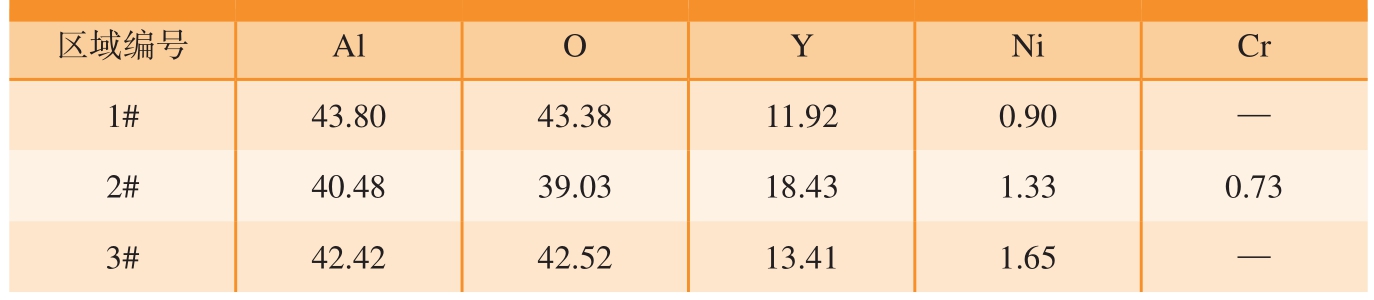
区域编号 Al O Y Ni Cr 1# 43.80 43.38 11.92 0.90 —2# 40.48 39.03 18.43 1.33 0.73 3# 42.42 42.52 13.41 1.65 —
图7(d)~(f)展示了3种涂层在1100 ℃氧化300 h后的样品截面图,3种涂层在长时间的高温热暴露过程中发生了明显的退化,原本弥散分布在退火态涂层中的黑色陶瓷颗粒相(图3(d)~(f))明显长大,在氧化后的涂层中形成了大量的陶瓷颗粒的团聚,经EDS检测这些黑色陶瓷颗粒相主要组成为Ni、Al和N元素以及少量的Cr和Co元素。通过对氧化后的涂层进行元素分析发现,在1100 ℃氧化300 h后涂层中的剩余Al质量分数分别为4.75%、5.10% 和 5.97%。从图7(d)~(f)中Al元素的分布图同样可以发现,随着O含量掺杂的增多,氧化后的涂层中残余富Al区域增多。产生这种现象的原因一方面可能是随着掺杂O含量提高,涂层中的陶瓷颗粒逐渐变多,细小的氧化物颗粒弥散分布在晶界与相界处抑制了涂层退化[24];另一方面,由于在1100 ℃下AlN的标准摩尔吉布斯自由能为–167.900 kJ/mol、Al2O3 为 –1237.552 kJ/mol。因此在氧化过程中Al2O3将通过以下方式在样品表面生成。
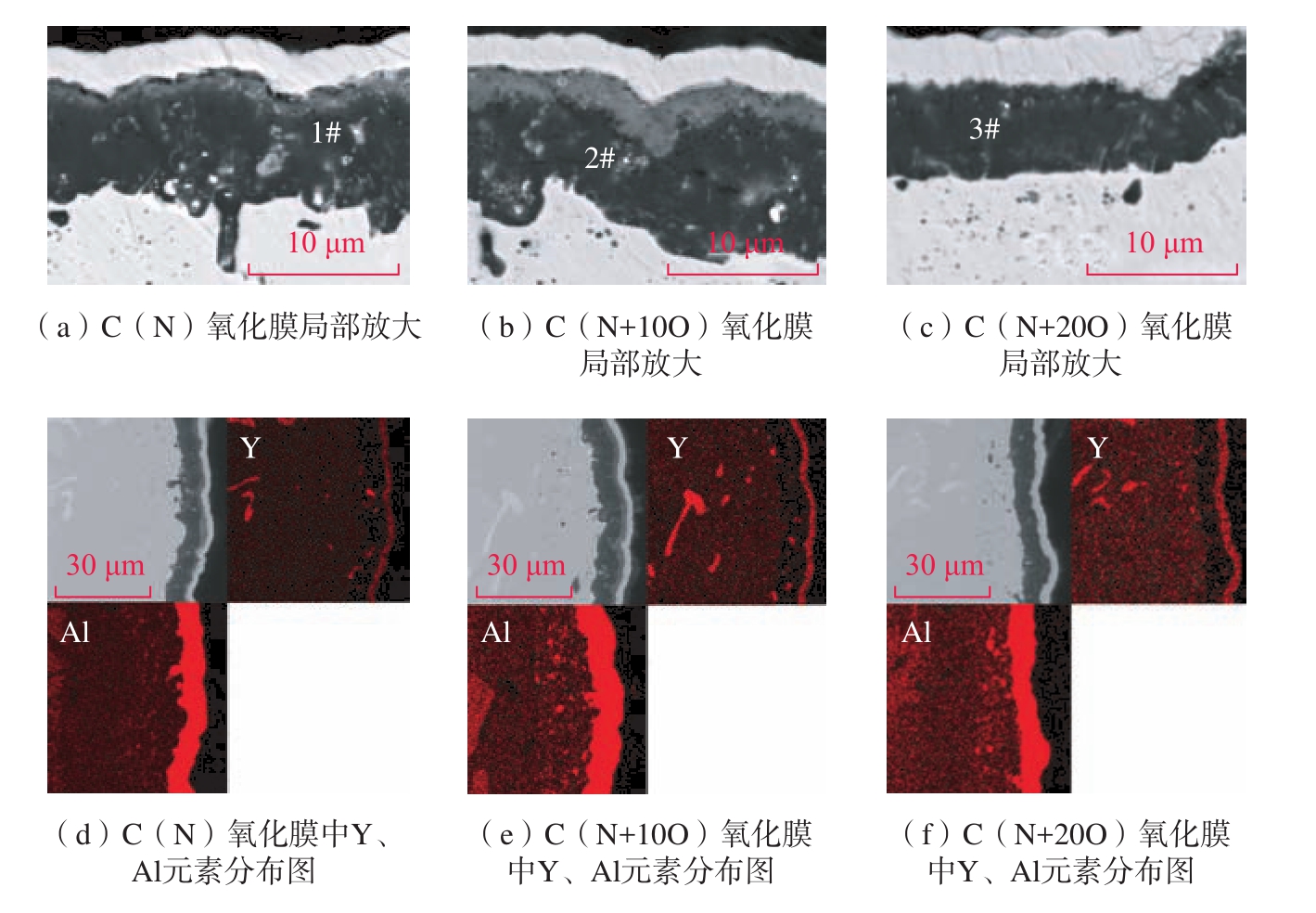
图7 3种涂层氧化膜局部放大图以及Y、Al元素分布图
Fig.7 Partial enlarged view of three kinds of coating oxide film and element mapping of Y and Al
AlN与O2反应后释放的N原子会与附近的金属Al反应再次生成AlN或以气体的形式向外释放[16]。由于N原子与Al有较高的亲和性,从而能促进涂层内部Al元素的上坡扩散[21],同时由于C(N+20O)生成的氧化膜较为致密完整,对Al元素的消耗较少,使得残余的富Al区域增多,从而提高涂层的抗氧化性能。但是掺入过多的O元素会造成涂层中大量的金属Al以Al2O3陶瓷颗粒的形式被固定在涂层中,对涂层的长期抗氧化性能造成不利影响,因此后期需要对涂层中掺入的O元素含量以及靶材中的Al含量进一步优化,使涂层获得更优异的抗氧化性能。
3 结论
使用多弧离子镀设备在二代单晶N5上沉积了具有不同O含量的纳米金属陶瓷涂层,研究其在1100 ℃下高温氧化性能,结论如下。
(1)C(N)、C(N+10O)和C(N+20O)制备态涂层中无明显的陶瓷颗粒析出,其主要的相组成为γ–Ni。当涂层在1000 ℃真空退火6 h后,涂层中析出大量的陶瓷颗粒,且随着涂层中掺杂O含量的提升,涂层中出现了大颗粒的陶瓷相。
(2)经1100 ℃的氧化测试300 h后,C(N)和C(N+10O)均生成了上层为NiAl2O4和下层为Al2O3的双层氧化膜,但C(N+20O)氧化膜并没有发生明显的分层。尖晶石相的生成会随着O含量的增加呈现先增加后减少的趋势。由于O对Y的拖拽作用,氧化膜中的富Y颗粒会随着掺杂O含量的增多而逐渐减少。
(3)氧化后,C(N)涂层几乎退化为金属涂层,C(N+10O)和C(N+20O)涂层中依旧残余较多的陶瓷颗粒。
[1]LI M H, ZHANG Z Y, SUN X F,et al.Oxidation behavior of sputter-deposited NiCrAlY coating[J].Surface and Coatings Technology, 2003, 165(3): 241–247.
[2]ZHAO P P, SHEN M L, GU Y, et al.High vacuum arc ion plating NiCrAlY coatings:Bias effect and approach to preparation of functional gradient coatings[J].Surface and Coatings Technology, 2015, 281: 44–50.
[3]SHEN M L, ZHAO P P, GU Y, et al.High vacuum arc ion plating NiCrAlY coatings:Microstructure and oxidation behavior[J].Corrosion Science, 2015, 94: 294–304.
[4]HOSSEINI S H, MIRDAMADI S,RASTEGARI S.Investigating efficiency of α–Al2O3 diffusion barrier layer in oxidation of EB–PVD NiCrAlY coatings[J].Surface Engineering,2015, 31(2): 146–155.
[5]GOTI R, BÉTAILLE–FRANCOUAL M, HOURCASTAGNÉ E, et al.Isothermal oxidation behaviour of NiCoCrAlYTa coatings produced by HVOF spraying and tribometTM process[J].Oxidation of Metals, 2014, 81(1–2):105–113.
[6]ZHANG B Y, YANG G J, LI C X, et al.Non-parabolic isothermal oxidation kinetics of low pressure plasma sprayed MCrAlY bond coat[J].Applied Surface Science, 2017, 406: 99–109.
[7]GIL A, NAUMENKO D, VASSEN R, et al.Y–rich oxide distribution in plasma sprayed MCrAlY-coatings studied by SEM with a cathodoluminescence detector and Raman spectroscopy[J].Surface and Coatings Technology, 2009, 204(4): 531–538.
[8]LU J T, ZHU S L, WANG F H.High temperature corrosion behavior of an AIP NiCoCrAlY coating modified by aluminizing[J].Surface and Coatings Technology, 2011,205(21–22): 5053–5058.
[9]VANDE PUT A, LAFONT M C,OQUAB D, et al.Effect of modification by Pt and manufacturing processes on the microstructure of two NiCoCrAlYTa bond coatings intended for thermal barrier system applications[J].Surface and Coatings Technology, 2010, 205(3): 717–727.
[10]YIN B, XIE G, LOU L H, et al.Effect of Ta on microstructural evolution of NiCrAlYSi coated Ni-base single crystal superalloys[J].Journal of Alloys and Compounds, 2020, 829: 154440.
[11]CHEN Y, ZHAO X F, XIAO P.Effect of microstructure on early oxidation of MCrAlY coatings[J].Acta Materialia, 2018, 159: 150–162.
[12]XIE S M, LIN S S, SHI Q, et al.A study on the mechanical and thermal shock properties of MCrAlY coating prepared by arc ion plating[J].Surface and Coatings Technology,2021, 413: 127092.
[13]ZHU L J, ZHU S L, WANG F H, et al.Comparison of the cyclic oxidation behavior of a low expansion Ni + CrAlYSiN nanocomposite and a NiCrAlYSi coating[J].Corrosion Science,2014, 80: 393–401.
[14]TAN X, PENG X, WANG F.The mechanism for self-formation of a CeO2 diffusion barrier layer in an aluminide coating at high temperature[J].Surface and Coatings Technology, 2013, 224: 62–70.
[15]BOLELLI G, CANDELI A,LUSVARGHI L, et al.Tribology of NiCrAlY+Al2O3 composite coatings by plasma spraying with hybrid feeding of dry powder+suspension[J].Wear, 2015, 344–345: 69–85.
[16]REN P, ZHU S L, WANG F H.Characterization and oxidation behavior of a sputtered nanocomposite Ni + CrAlYSiHfN coating[J].Corrosion, 2015, 71(4): 523–535.
[17]REN P, YANG Y F, ZHU S L, et al.Effect of Ti on the microstructure change and oxidation behavior of Ni + CrAlYHfSiN composite coatings[J].Corrosion Science, 2019,150: 54–63.
[18]REN P, ZHU S L, WANG F H.Microstructural stability of AlN diffusion barrier for nanocomposite Ni + CrAlYSiHfN coating on single crystal superalloy at high temperatures[J].Applied Surface Science, 2015, 359: 420–425.
[19]LIU Z L, SHEN M L, ZHU S L, et al.Oxidation mechanism of a nanocrystalline NiCrAlYSiHfN/AlN multilayer coating[J].Corrosion Science, 2019, 156: 71–83.
[20]REN P, ZHU S L, WANG F H.TEM study of the evolution of sputtered Ni +CrAlYSiHfN nanocomposite coating with an AlN diffusion barrier at high temperature[J].Surface and Coatings Technology, 2016, 286:262–267.
[21]JIA Y X, ZHU S L, LIU Z L, et al.Oxidation mechanism of Ni + CrAlYNO nanocomposite coating enhanced by a NiCrAlY buffer layer[J].Corrosion Science, 2021, 180:109184.
[22]CHEN W R, WU X, MARPLE B R,et al.The growth and influence of thermally grown oxide in a thermal barrier coating[J].Surface and Coatings Technology, 2006, 201(3–4): 1074–1079.
[23]YAO H R, BAO Z B, SHEN M L,et al.A magnetron sputtered microcrystalline β–NiAl coating for SC superalloys.Part II.Effects of a NiCrO diffusion barrier on oxidation behavior at 1100 ℃[J].Applied Surface Science,2017, 407: 485–494.
[24]JIA Y X, ZHU S L, LIU Z L, et al.Effects of oxygen incorporation in low expansion Ni + CrAlYN nanocomposite coatings on the oxidation behavior[J].Corrosion Science,2020, 167: 108550.
